
Током деветнаестог века, снажна реформацијапрошли су много праваца, укључујући и хемију. Мендељејев је периодични систем, формулисан 1869. године, довела је до заједничког разумевања односа између положаја једноставних материја у периодном систему, да се успостави однос између релативне атомске масе и Валентност елемент имовине.
Неколико раније, почетком деветнаестог века,направљени су поновљени покушаји да се систематизују хемијски елементи. Немачки хемичар Добереинер водио је први озбиљан рад на систематизацији у области хемије. Утврдио је да се мноштво сличних супстанци по својствима могу комбиновати у групе - триаде.
Суштина представљеног закона тријада Добереинер-а одређена је чињеницом да је атомска маса траженог супстанца близу полувремена (просечна вредност) атомских маса последња два елемента тријад стола.
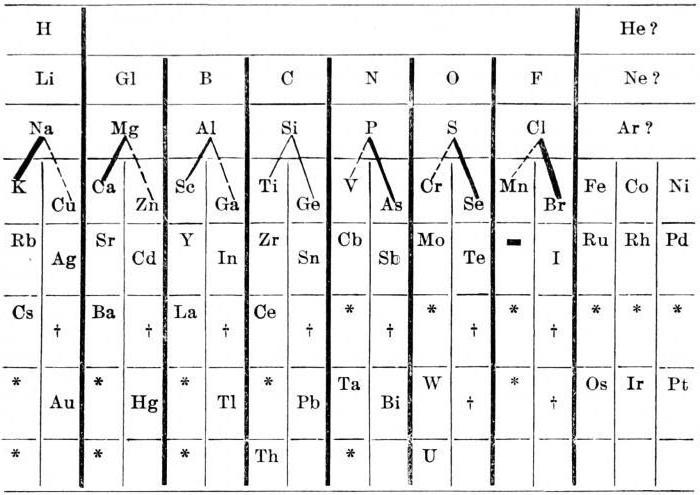
Овај приступ је резултат вештачкогограничења сличних супстанци само тројни синдикати. Јоханн Волфганг Добереинер могли да виде сличности у хемијских параметара фосфора и арсена, бизмута и антимона. Међутим, ограничио се на потрагу за тријадама. Као резултат тога, он није могао да дође до тачне класификације хемијских елемената.
Раздвојите постојеће елементе у триадеДоуббереир свакако није успео, закон јасно указује на присуство везе између релативне атомске масе и својстава хемијских једноставних супстанци.
Сљедећи покушаји систематизације су се ослањалио расподели елемената зависно од њихове атомске масе. Касније, хипотеза Добереинер-а су користили други хемичари. Појавило се формирање триада, тетрадова и пентада (груписање у три, четири и пет елемената).
У другој половини деветнаестог века појавио сеу исто време неколико радова, на основу којих је Дмитриј Ивановић Менделеев доводио хемију у пуну систематизацију хемијских елемената. Различита структура периодичког система Менделејева довела је до револуционарног разумевања и очигледног механизма дистрибуције једноставних супстанци.
На састанку руског хемијског друштва у пролеће 1869. је прочитао обавештење на руском научнику Мендељејев о свом открићу периодичног закона хемијских елемената.

У новембру 1870. године својим колегама је додао додатак"Природни систем елемената и његова употреба за означавање квалитета неоткривених елемената." У овом раду ДИ Менделејев је први користио појам "периодични закон". Систем Менделеевских елемената на основу периодичног закона утврдио је могућност постојања не отворених једноставних супстанци и јасно показивао њихове особине.
Као резултат тога, до 1971. године, периодични закон и периодични систем Менделејева елемената су пречишћени и допуњавали руски хемичар.
У завршном чланку "Периодична законитостхемијски елементи ", научник је утврдио дефиницију периодичног закона, у којем се наводи да су карактеристике једноставних тијела, особине једињења и сложена тела која их формирају, одређена директном зависношћу према атомској тежини.
Неколико касније, 1872. године, структура Менделејевевог периодичног система реорганизована је у класичан облик (краткотрајни начин дистрибуције).

За разлику од својих претходника, руски хемичар је направио сто у потпуности, увео концепт правилности атомске тежине хемијских елемената.
Карактеристике елемената периодичне таблицеМенделејев и изведене законитости дозвољавали су научнику да опише својства елемената који још нису отворени. Менделеев се ослањао на чињеницу да се својства сваке супстанце може одредити према карактеристикама два суседна елемента. Назвао га је владавином "звезде". Његова суштина лежи у чињеници да је у табели хемијских елемената за одређивање својстава изабраног елемента потребно хоризонтално и вертикално усмерити у таблу хемијских елемената.
Табела Менделеевских елемената, упркос њеномтачност и верност, научна заједница није у потпуности признала. Неки од великих свјетски познатих научника отворено су исмијавали могућност предвиђања особина неоткривеног елемента. Тек 1885. након открића предвиђених елемената - ЕКА-алуминијума и екабора екасилитсииа (галијум, скандијума и германијума), нови систем класификације за Менделеев је периодичног закон и препознати су као теоретским основама хемије.
На почетку двадесетог века, структура периодичногСистем Менделејева је више пута коригован. У процесу добијања нових научних података, ДИ Менделејев и његов колега У. Рамсаи дошли су до закључка да је неопходно увести нулту групу. Укључени су инертни гасови (хелијум, неон, аргон, криптон, ксенон и радон).
Године 1.110, Ф. Содди предложио је да се у једну ћелију стола постављају неодвојиви хемијски елементи - изотопи.
У процесу дугог и малог посла, столапериодични систем хемијских елемената Менделејев је завршен и стекла модеран изглед. То је укључивало осам група и седам периода. Групе су вертикалне стубове, периоди су хоризонтални. У групама је дефинисана подела на подгрупе.
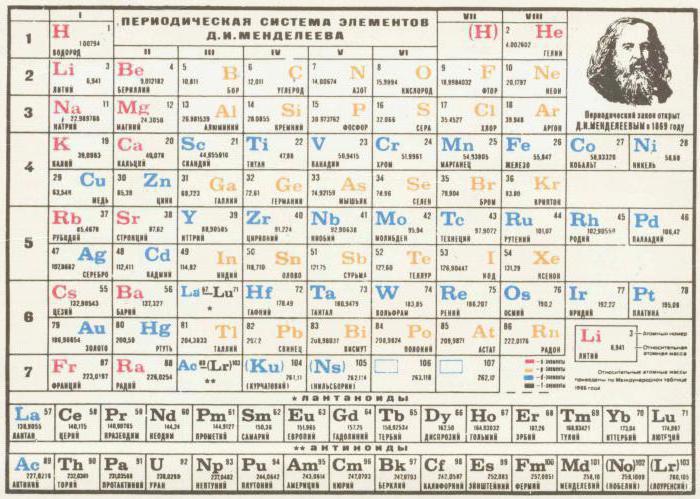
Положај елемента у табели означава њенуваленце, чисте електроне и хемијске особине. Као што се касније показало, током развоја табеле, ДИ Менделеев је открио случајну коинцидацију броја електрона елемента са својим серијским бројем.

Систем Менделејева и његов приступ наручивањухемијски елементи унапредили су даљњи развој хемије. Захваљујући тачном разумевању односа између хемијских константи и анализе, Менделеев је могао правилно груписати и груписати елементе према својствима.
Откриће руског научника имало је директан утицајо даљњем развоју науке и технологије. Не постоји технолошка област која не укључује познавање хемије. Можда, ако се таква открића није догодила, наша цивилизација би пратила другачији пут развоја.
</ п>